
医疗器械注册文件,千万别造假
一句话先说结论:
👉 医疗器械注册文件,不是“申报材料”,是“法律文件”。
👉 造假,不是退回,是撤证。
最近两年,监管态度已经非常明确。

产品:一次性使用气管插管
注册证号:苏械注准20182081539
结果:撤销医疗器械注册证,罚没所得,10年内不再受理医疗器械许可申请
依据:《医疗器械监督管理条例》第八十三条第一款(并援引行政许可法)

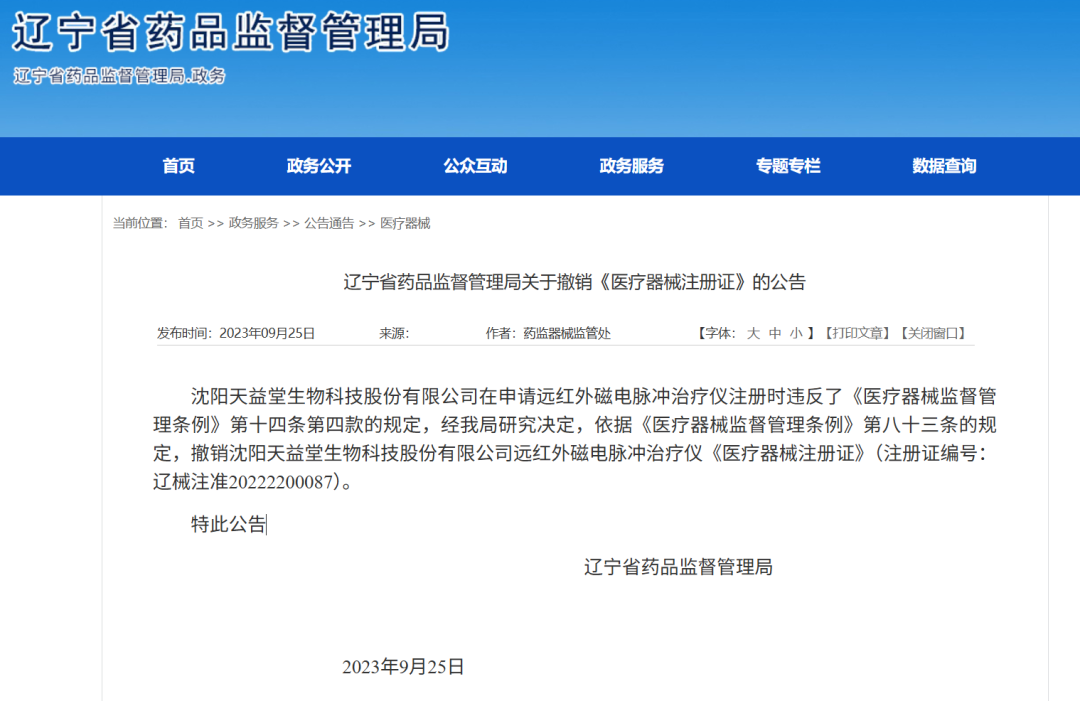
产品:远红外磁电脉冲治疗仪
注册证号:辽械注准20222200087
结果:撤销医疗器械注册证
原因:申请注册证违反了《医疗器械监督管理条例》第十四条第四款的规定
你要看清的,不是“案例”,而是趋势
这三起案件,有几个高度一致的信号:
❌ 不是“质量问题”
❌ 不是“不良事件”
❌ 不是“临床失败”
而是——
⚠️ 注册文件不真实 / 提供虚假资料
监管已经反复用行动说明:
只要触碰“虚假申报”,不谈改正空间,直接否定许可资格。
注册文件,本质上是什么?
请所有医疗器械从业者记住一句话:
你递交的注册资料,是对国家监管机构作出的正式法律陈述。
不是PPT
不是内部汇报
不是“差不多就行”
而是:
可被追责
可被倒查
可直接撤销行政许可
给不同岗位:今天就能落地的行动清单
给医疗器械老板
把“注册资料合规”列为红线项目:资源、时间、责任到人
一句话:别用业绩KPI去逼出合规事故!!!
给注册/法规(RA)
建立“关键声明清单”:凡是写进申报资料的承诺,都要能证明
把第八十三条当“底线条款”去做培训与签
给质量(QA)
重点盯:记录真实性、供应商控制、外包过程、数据完整性
让“审评资料”与“体系现场”一致!!!不要两套系统
给研发(R&D)
别只交PPT式结论。把验证、确认、风险管理证据链补齐
每次变更都要问:这会不会影响申报承诺?
给临床/医学(CM/MA)
临床评价不是写作比赛,是证据逻辑比赛
同品种选择、差异分析、适用性论证,越关键越不能模糊
最后一句提醒(请你原文保留)
医疗器械注册文件,一页都不能造假。
因为代价不是“重做资料”,而是——注册证撤销。
如果你所在的企业正在:
做注册
补资料
准备变更
或已经上市多年
👉 现在,就是最该回头检查注册文件真实性的时候。

