
FDA 2026年用户费涨价,出口美国的企业得留意成本变化
FDA前阵子在联邦公报上发布了2026财年医疗器械用户费标准,年度机构注册费定在11,423美元,比上年涨了点。申请费也相应调整:PMA标准费579,272美元,小企业优惠144,818美元;510(k)标准费26,067美元,小企业优惠6,517美元。简单算下来,一家中小企业如果涉及机构注册和一个510(k)申请,额外开支可能多出几千美元。 
国内出口企业反馈,这波变化会加重负担,尤其是小厂家,合规费用本来就占比例。现在FDA的总目标收入调整到约4.28亿美元(基础3.66亿,经通胀上浮),加上绩效改善调整的5,033万美元,总预期收入近4.78亿美元。这些钱主要用于审评团队薪资、设施维护和运营,支持更快更高效的器械审批。  但对企业来说,意味着美国市场门槛在抬高。
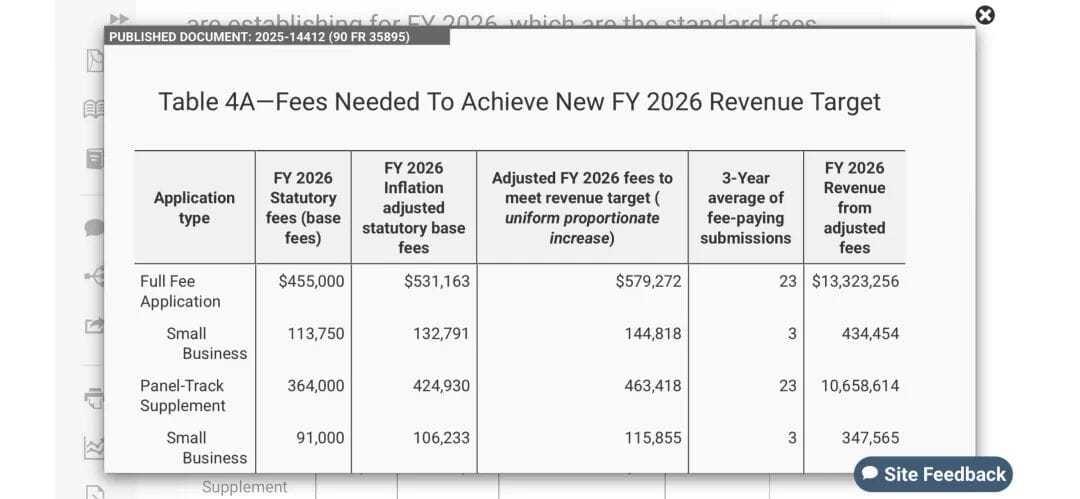
对比NMPA收费,差距明显。NMPA进口Class II初始注册费21.09万元人民币(约27,000美元),Class III 30.88万元(约39,000美元)。变更注册Class II 4.2万元,Class III 5.04万元,每5年续展4.08万元。没有年度机构费。周期上,NMPA Class II 16-24个月,Class III 24-36个月,费用整体更易把控。FDA的PMA是NMPA Class III的10倍多,还年年缴注册费。当然,美国市场大,回报高,就看前期投入怎么平衡。
从经验看,以下几点或许有用:
• 预算时,评估产品分类。高风险Class III涨幅影响大,低风险Class I/II豁免多。小企业(营收<1亿美元)申请优惠,能省75%;如果营收<3,000万美元,第一笔PMA可能全免。
• 申请中,减少补件。QMSR 2026年2月生效,对齐ISO 13485能提升效率。
• 资源上,De Novo适合创新器械,费用低。看看FDA指导或国内协会分享。
• 市场布局,如果美国成本高,欧盟MDR有简化讨论,或者专注国内,NMPA亲民。
这是MDUFA V协议的延续,每五年审视。一些企业通过聚焦高值产品或优化链条,适应下来。如果有经验,评论区交流。

