
MDR CER 的机遇与挑战?
 。其中Article 61-10 performance 临床评价路径更是业内公说公有理婆说婆有理的一个极具争议的话题,那今天就来一起argue 一下Article 61-10 performance 临床评价的神秘面纱,求同存异,希望可以给需要的伙伴带来一些思考或思路~
。其中Article 61-10 performance 临床评价路径更是业内公说公有理婆说婆有理的一个极具争议的话题,那今天就来一起argue 一下Article 61-10 performance 临床评价的神秘面纱,求同存异,希望可以给需要的伙伴带来一些思考或思路~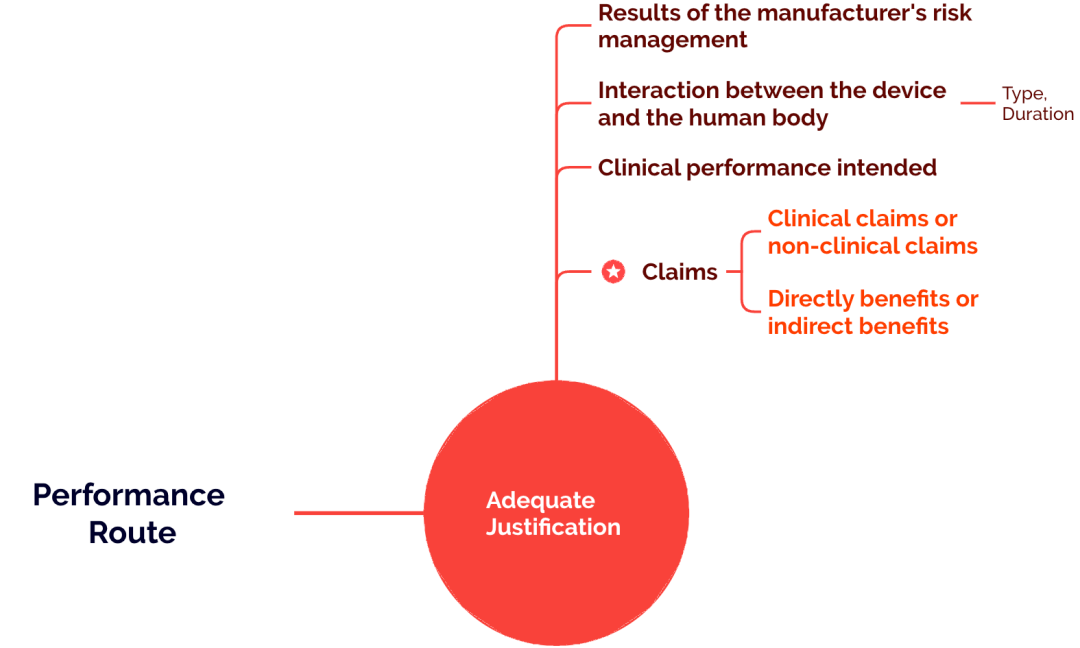
1. Article 61-10 的来源与核心考量?
2. 哪些器械可以走article 61-10?
3. 哪些数据可支持 performance 路径?
4. Performance 路径的“功”与“过”?
1. Article 61-10 的来源与核心考量
根据MDR CHAPTER VI Article 61 Clinical evaluation 第10条,业内也叫article 61(10),原文旨意是如果认为通过临床数据证明器械的安全性和性能是不适合的,可考虑用器械performance 路径完成临床评价,但是制造商必须要给出一个Adequate Justification,其应基于以下关键考量因素
风险管理的结果
器械与人体接触的情况(接触方式,接触时间,相互作用的新颖性)
制造商intended clinical performance
Claims(尤其是与临床相关的claims)
其中,在做欧盟临床评价是否可以走performance 路径的主要判断核心或者说是“分水岭”,是要判断目标器械是否有直接的临床受益的claim(direct clinical benefits claims),这个是主要判断依据。有时候往往做这样的判断有些困难,当你迷茫时不妨从这几个角度考虑出发:
Device has direct influence on clinical outcomes or not?
The clinical benefits can be specified through measurable or not?
Positive impact on Patient-relevant healthe/ clinical outcome(s)?
The clinical benefit is direct OR indirect?
需注意,以上可以考虑走performance路径器械的前提是非植入类或三类器械(且这类器械必须要做临床试验)的器械。
聊完规则,大家可能更好奇的是究竟哪些器械我可以走performance路径完成我的临床评价,那么接下来就看看目前的一些实例 (不同NB maybe have difference opinions),相信以后还会根据行业内企业与公告机构不断的实践会不断有更新~
2. 到底哪些器械可以走article 61-10 performance 临床评价路径?
我们都想明确的知道到底哪些器械可以走Article 61-10以便作为参考来判断自己的器械是否也可以?
在此之前需要强调的是Article61-10 路径不是没有临床数据的“借口”或“捷径”,比如,我们的器械很简单运行很正常,几乎没有抱怨?没有人会专门针对我们的器械做相关研究,因为只是个辅助工具?临床文献检索检索不到相关的文献?(Absence of evidence is not evidence of absence)
而是基于器械本身的设计和预期用途实质,确实认为临床数据是不需要的,就可以证明器械的安全性和有效性。比如以下是目前根据实践经验整理的一部分可以走performance clinical evaluation 的器械总结与整理:
器械类别 | 示例 | 考量因素 |
实验室设备 | 血液冷藏箱、实验室天平、离心机 | 不与患者直接接触,无临床获益 |
基础外科手术工具、部分WET器械 | 镊子、剪刀、止血钳,牵引器,金属丝、针、小夹和连接体等低风险器械 | 与人体接触但无能量交换,设计成熟 |
牙科设备 | 牙科治疗台、口角器,口镜 | 低风险,结构功能为主 |
辅助类设备 | 轮椅、助行器、病人定位系统,手术灯,医用冰袋,固定绷带等 | 机械结构为主,无治疗功能 |
部分独立软件 | 不直接影响诊断或治疗决策的辅助软件 | 无诊断或治疗性声明 |
无源测量设备 | 听诊器,血糖仪(非诊断性)、体温计 | 若未声称临床获益,可考虑61(10) |
器械附件 | 不直接影响主设备性能的配件,如导管附件,耗材配件 | 无独立临床声明,仅功能性验证 |
主机类 | 比如某些球囊导管和主机配合使用的主机只提供能量 | 只提供能量,无直接临床受益 |
医用耗材 | 注射器,导管(tube not catheter),辅料,超声偶合剂,牙科印模材料,非植入式引流管,清洁剂或消毒剂, | 无直接临床相关受益相关的声明 |
低分险康复设备 | 助行器,拐杖等 | 仅功能性宣称 |
低风险监护设备 | 体温探头等 | 仅功能性验证 |
辅助诊断影像类设备 | 仅提供医学影像学图像 | 无直接诊断性或治疗性等临床相关的宣称 |
3. 如果可以走performance 路径,究竟哪些数据可以可用来证明你的器械的安全和性能?
Bench testing
Common specifications, Harmonized standards related test
Pre-clinical data
such as mechanical testing for strength and endurance, biological safety, usability, etc
Performance data
Verification&Validation, Volunteer test, animals test, Simulated use / animal / cadaveric testing involving healthcare professionals or other end users
PMS/Vigilance Data (If device has previously been marketed)
Include PMCF data
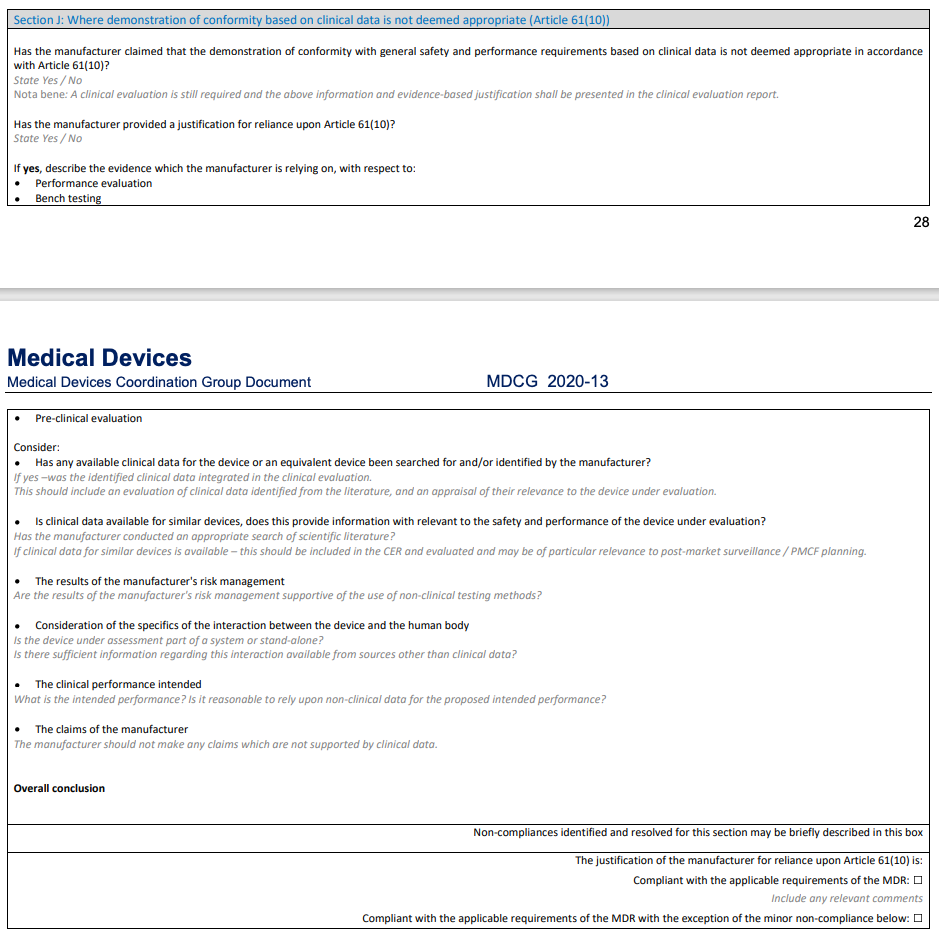
具体操作实践指南可参考MDCG2020-13 Section J (作为Article 61-10临床评价的要求和checklist)
4. 为什么说performance 临床评价既是机遇也是挑战呢?
当看到这个话题有些伙伴可能要来dis 小编了,WHAT!,欧盟MDR CER哪还有什么机遇,处处是挑战啊啊啊?!
当然,所谓“机遇”是有条件的,比如说在上面提到的相对分险较低且认为临床数据证明器械的安全性和性能是不合适的器械,对于这类器械,无疑performance 临床评价路径就是机遇。既然是机遇,那就有一定的“好处”,比如豁免临床试验为低风险医疗器械带来显著合规红利与效率提升,其核心价值体现在监管适配性优化、成本与周期压缩及技术成熟产品的快速转化三方面,但是,同时,若需证明你的器械可以走performance 临床评价路径,往往需要更严谨的分析和设计,要有充分的Justification和自洽的逻辑证明“你的器械行”,难就难在咱们很多时候自己无法做出科学(这里往往需要一些有临床医生背景的专业输入)正确的判断,且同时无法向“NB机构”证明我们的器械行,所以今天小编整理了一些实操成功经验的分享,希望可以帮助到还在为performance 临床评价路径纠结的你提供一些参考或思路~
还需强调,走performance 路径不代表可以不写CER,且CEP,CER, PMCF, PSUR 等该有的都少不了,并且performance 路径临床评价不代表可以不检索和分析文献,也不代表整个临床评价报告中不能出现“临床证据”,其中SOTA和GSPR的证明还是少不了,详情请参照以上MDCG 2020-13 Section J所给的指导意见。
最后小编还想说句掏心窝子的话,临床评价策略一定要先行,临床评价不仅仅是一份临床合规报告,也不是一份宣称器械能干啥的报告,而是要证明器械可以干啥和怎么样的一个围绕器械全生命周期的一个过程;强烈建议在R&D 之前就应该制定好器械的临床评价策略,而不是等产品都成型了,该做的验证或测试都做完了,才开始在一堆数据和文件中“堆砌”出一个 “包罗万象”的临床评价报告,临床评价是一个“自证清白”的机会啊!!!一定是有主线,有逻辑,环环相扣的 “可证明你的器械可行的一个临床故事~“
最最最后,为了今天的主题不跑题,再啰嗦一下所谓的performance临床评价路径的挑战,如果有企业或器械有的是钱,不怕烧钱,为了临床市场推广,也会做一个临床试验作为市场的推广的背书,所以如果是走performance 路径,就不可以有明确的真实的“clinical claims”,有些人会认为对产品市场宣传和推广是不利的,但是,小编认为,还是要回归器械的本质,“clinical claims”有就是有,没有就是没有,不会因为你做了临床试验就可以beyond the intended purpose 而产生所谓的“clinical claims”。
最后的最后,到这里有些小伙伴就会冒出一个灵魂拷问,那么,如果是走了performance 临床评价路径,那我的整个临床评价的“灵魂” - Safety and performance parameters and acceptance criteria & SOTA 又该从何而来?这个是好问题,留个彩蛋见下回分晓~
Reference



