【政策解读】英国临床试验,最快 7 天批准

Route B 到底是个啥?

调整一下入组标准 更新一下知情同意书版本 增加两位研究者
平均审批时间:7 天 自动通过比例:89% 被叫停比例:11%(主要因为材料不全)
什么项目能走?什么不能?
访视频次调整(比如从 3 次改成 5 次) 招募策略微调(扩大年龄范围) 伦理委员会人员变更 知情同意书文字优化 数据管理计划更新
主要终点变更 器械设计或规格修改 受试者安全相关的操作流程调整 方案核心部分大改
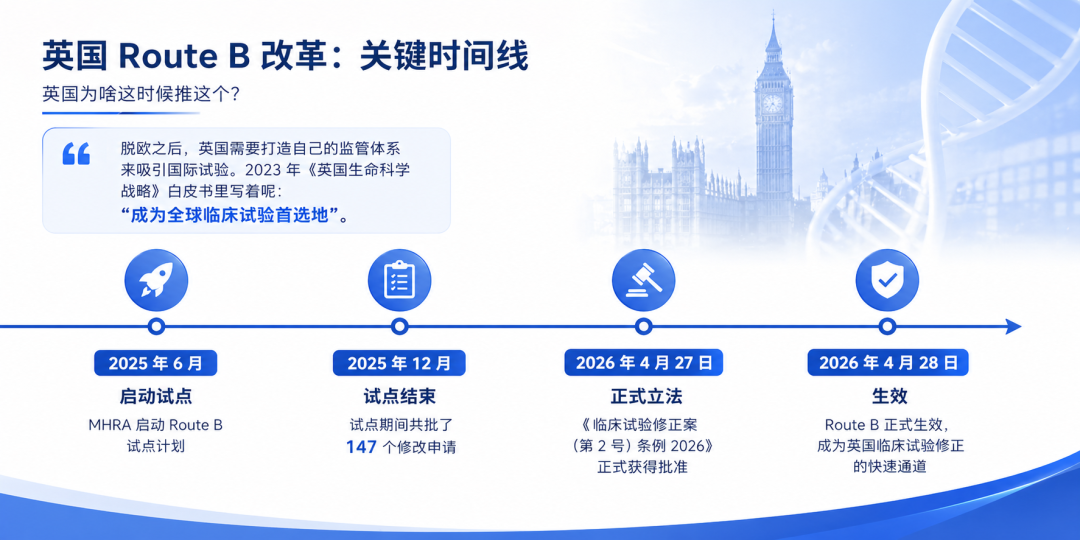
英国为啥这时候推这个?
2025 年 6 月:启动试点 2025 年 12 月:试点结束,批了 147 个修改申请 2026 年 4 月 27 日:正式立法 2026 年 4 月 28 日:生效
美国 FDA:有突破性设备通道,但整体周期还是长,平均 12-18 个月 欧盟:CTIS 统一评估 60 天,但流程复杂,常超期 日本 PMDA:早期对话机制不错,适合创新器械,但文件要求细
做英国项目,真实成本是多少?
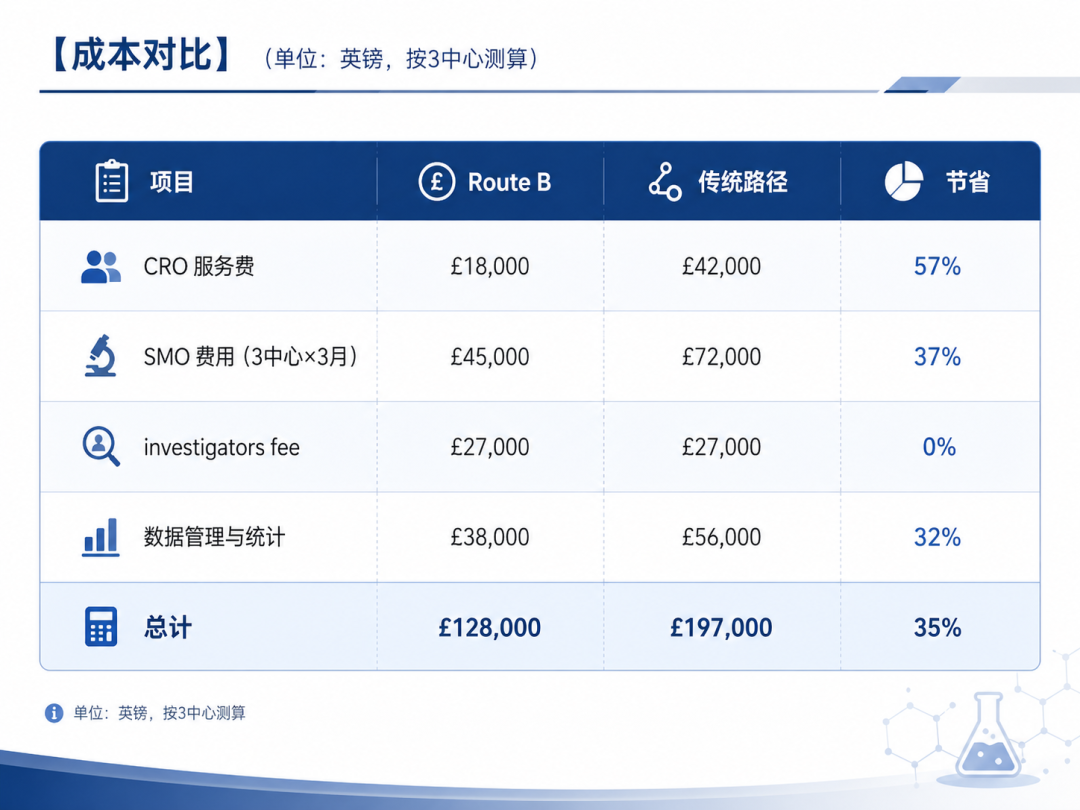
**前期预审**:自己团队或找顾问把材料先过一遍,避免被叫停。我们建议花 £5,000-£10,000 做预审。 **沟通成本**:MHRA 可能会提问,你得在 24-48 小时内回复。伦敦办公室有时差,最好本地有对接人。
小公司怎么控制?
核心流程(提交、跟进)可以外包,但伦理沟通尽量自己做 用我们的模板清单自检,省掉顾问费 分阶段付款:提案通过付 30%,MHRA 受理付 40%,获批后付 30%
被 MHRA 叫停怎么办?
试点里 11% 被叫停,主要原因:
伦理文件不完整(占 40%) 知情同意书有问题(30%) SAE 报告机制没写清楚(20%) 方案偏离没记录(10%)
24 小时内内部开会,明确谁补什么 72 小时内补交(拖久了 MHRA 会认为你不上心) 如果补交后 15 天 MHRA 没回复,主动打电话问 一般会给 15 天宽限期
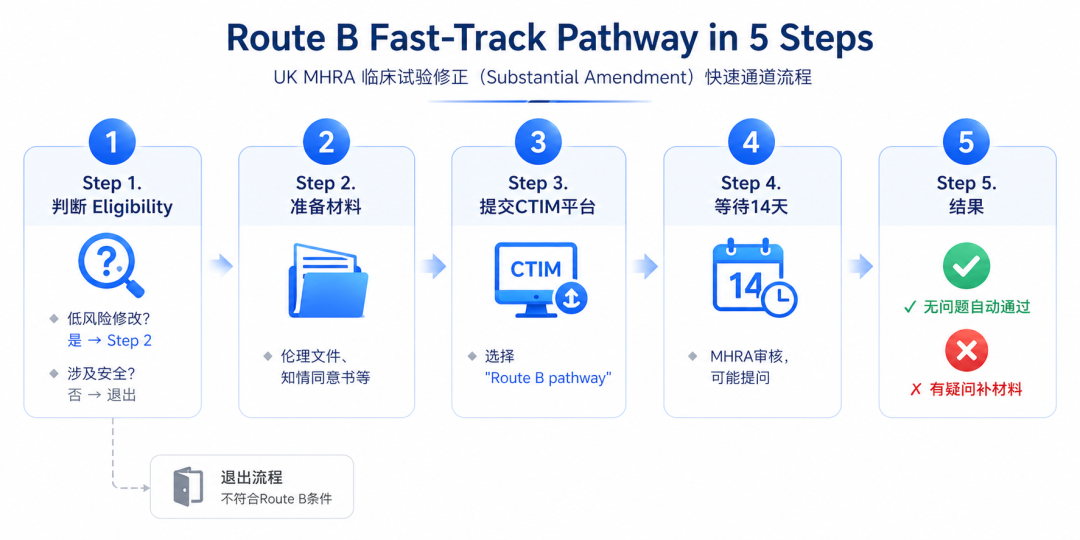
你自己项目,到底能不能走 Route B?
我整理了 5 个问题,你可以先自己过一遍:
**改动影响受试者安全吗?** → 不影响 **属于低风险修改吗**(招募、知情、人员)→ 是 **材料能一次交齐吗?** → 能 **已有伦理委员会批准吗?** → 有 **14 天内能响应 MHRA 提问吗?** → 能
三类器械要格外小心
涉及器械设计变更的修改,基本不能走 Route B 但像访视频率调整、入组标准放松这类,可以
70% 的修改符合 Route B IVD 试剂尤其合适
小版本迭代(比如检测算法微调)可以走 Route B 大版本或机器学习模型重训练,可能要重新审批
联合申报,MHRA 要和 EMA 协调 建议提前 6 个月启动沟通
说点实际的:你要准备什么?
伦理委员会批准文件(版本、日期要对) 知情同意书(最新 signed copy) SAE 报告流程(24 小时联系人写清楚) 方案偏离记录表格(最近 3 个月的) 数据管理计划(包括数据锁定时间) 研究者资质文件(GCP 证书、CV) 保险凭证(临床试验责任险) 器械临床试验备案文件(如果适用)
你的项目到哪一步了?
已启动,正在找 CRO 计划中,在评估方案 观望中,再等等看 不考虑,专注国内
最后说几句


