
Apple Watch房颤功能终获NMPA二类认证:可穿戴医疗器械赛道的新风口与实操启示
最近刷到一条重磅消息:苹果的“移动脉率房颤迹象记录软件”(也就是Apple Watch的Atrial Fibrillation History Feature)在2025年12月26日正式拿下NMPA进口二类医疗器械注册证,证号国械注进20252210606。这不是整个手表获批,而是针对房颤监测这项软件功能,专为22岁以上已确诊房颤患者设计,能回顾性估算房颤发作时长比例,并与生活方式数据关联分析。苹果官方回应说,正在走正规流程,很快就能在中国落地使用。
作为医疗器械圈里的老鸟,这事儿让我眼前一亮。苹果从2018年FDA清关ECG功能开始,就在可穿戴医疗上玩得风生水起,但国内市场一直卡在NMPA门槛上。现在终于过关,意味着大厂们正加速把消费电子往医疗器械转型。这对我们从业者来说,是个信号:可穿戴设备不再只是“健康追踪器”,而是能合法进入临床辅助的工具。想想看,房颤患者日常监测房颤负荷(发作时长占比),不用总跑医院,这能极大提升患者依从性和数据连续性。但别高兴太早,二类注册的门槛不低——从临床验证到数据算法可靠性,都得过硬。

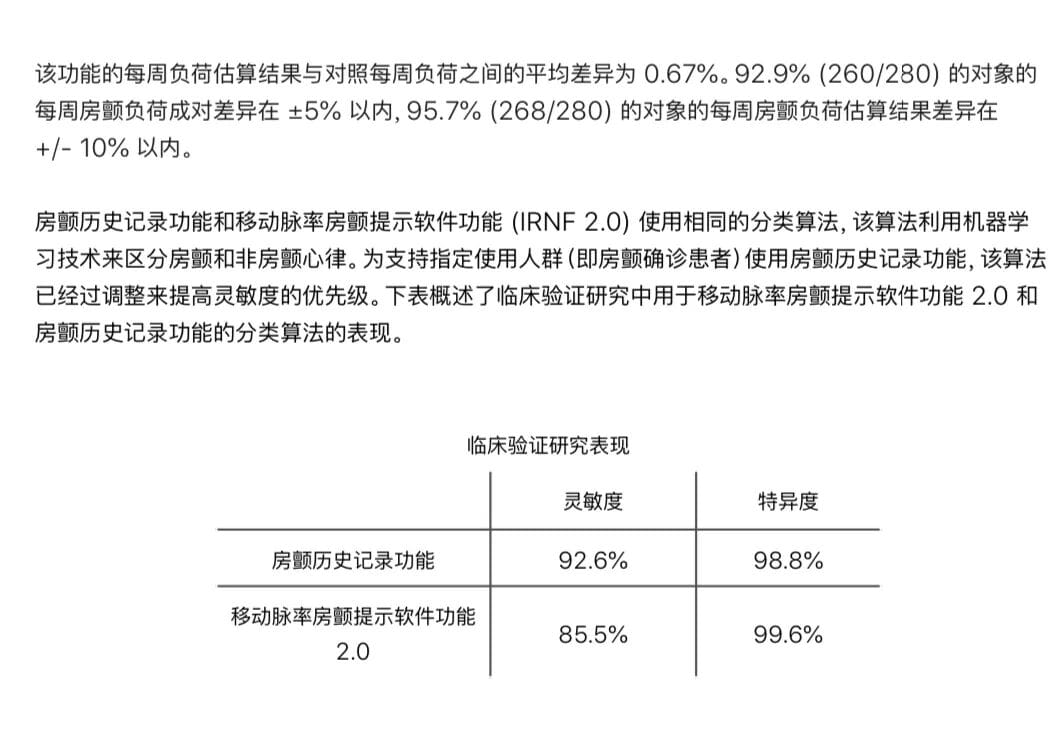
从市场角度评估,这会刺激国内可穿戴医疗器械的竞争。华为、OPPO等早几年就拿下类似ECG认证,现在苹果跟进,预计2026年这类产品销量会再翻番。但挑战也明显:NMPA对软件算法的bias控制、数据代表性要求越来越严,单纯的回顾性数据很难过审,得结合前瞻性临床试验或RWD(真实世界数据)来补强证据。举个例子,我们之前帮一家本土智能手环企业做二类注册时,就发现算法在亚洲人群的敏感性/特异性数据不足,导致补正了好几轮。最后用hybrid证据策略(RCT小样本 + 多中心RWD)才顺利通过,缩短了半年周期。
如果你是申办方或初创团队,正盯着类似AI-enabled可穿戴项目,这事儿给的启示是:别只盯着技术创新,得早早布局监管路径。NMPA二类注册的核心痛点在于临床评价报告(CER)和软件验证,尤其是针对慢性病监测的功能,得证明不只是“提示”,而是可靠的“记录”。机遇在于,政策在鼓励数字化转型,像房颤这类高发疾病的辅助工具,市场空间巨大——据估,国内房颤患者超千万,日常监测需求正爆棚。

