ISO15223过渡期确定:审核会问
知道更新吗? 知道截止日吗? 有适配计划吗?
1 先看结论:FDA 写了“过渡期”,不是传言
别再靠转述,FDA 在认可共识标准数据库里明确录入:
ISO 15223-1 第四版 2021-07,包含 AMD1:2025(Rec# 5-148),录入日期 2025-12-22。
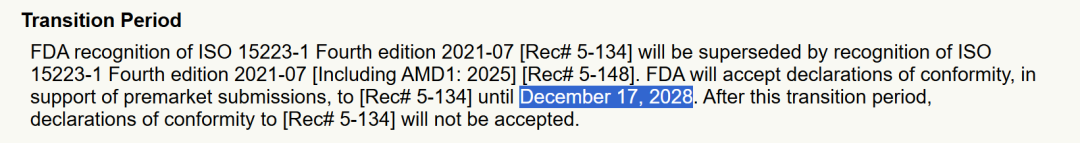
旧识别版本(Rec# 5-134)的符合性声明可被接受至 2028-12-17;之后不再接受旧版声明。
一句话:你可以按节奏切换,但你不能装作没发生。
2 AMD1:2025 更新内容?为什么会变成“审核话题”
很多团队第一反应是:符号嘛,改改图标就完了。
但这次更新的信号更明确:标准在把“代表信息/符号表达”从区域化,推向更通用的表达。
ISO 对 AMD1 的核心描述包括:
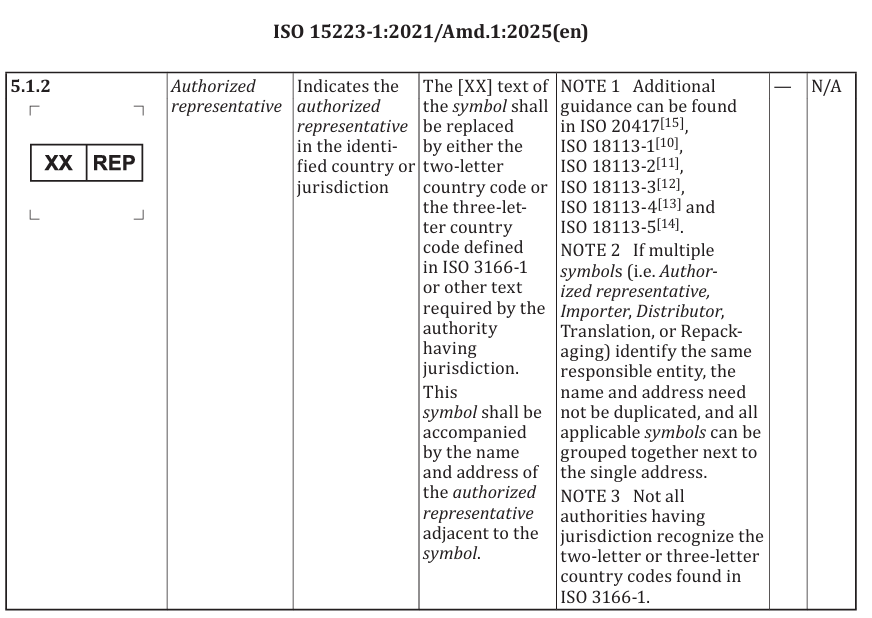
新增“授权代表”相关定义术语
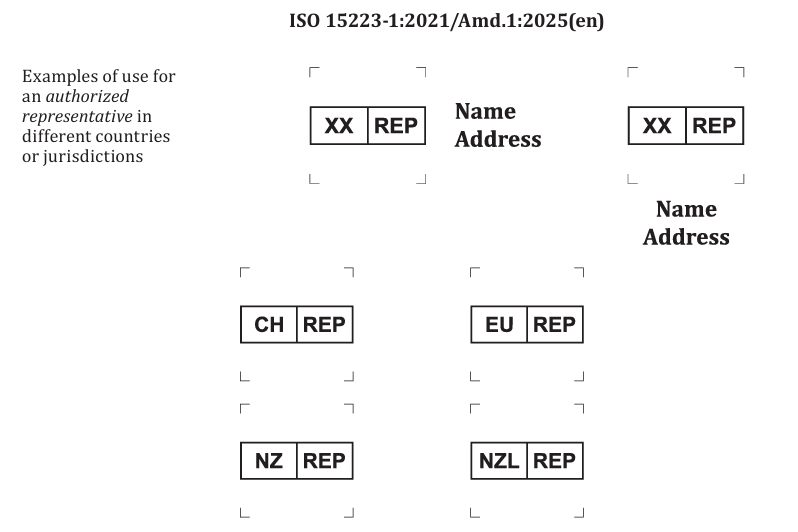
修改原本偏“EC-REP”语义的代表符号,使其不再绑定特定地区
这会触发审核员的自然追问:
你们的标签策略是否还停留在旧理解?
多法域代表信息怎么一致管理?
变更证据链有没有?
3 为什么现在可能“不要求你立刻改”,但审核会“立刻问”
因为过渡期保护的是实施窗口,而审核看的是管理能力。
你只要站在审核员视角想一遍就懂了——他们不会问“你换没换”,他们会问“三连”:
1)你知道标准更新了吗?
2)你知道 FDA 过渡期截止到哪天吗?(2028-12-17)
3)你有适配计划吗?谁负责?什么时候完成?证据在哪?
如果你回答含糊,接下来就会升级成体系问题:
标准监测机制是否有效
文件控制是否闭环
标签/IFU/技术文件是否一致
4 不知道、没计划,会有什么现实风险?
我建议你把下面这句写进 部门会议PPT:
“过渡期越长,越容易被误以为可以不管。”
常见风险不是“一条符号开大项”,而是连锁反应:
被质疑法规监测/标准清单更新机制失效
被要求补充影响评估、变更记录、培训证据
临近截止日集中切换,供应链、包材、注册变更一起拥堵
5 送你一段“审核现场最稳的回答”(建议)
问:你们知道 ISO 15223-1 更新吗?
答:知道,我们已将 ISO 15223-1:2021(含 AMD1:2025)纳入适用标准清单,并完成影响评估与实施计划。
问:FDA 过渡期到什么时候?
答:FDA 接受旧识别版本 Rec# 5-134 的符合性声明至 2028-12-17,之后不再接受旧版声明。
问:你们什么时候完成切换?
答:我们按“新增/变更优先、存量分批切换”执行,并设置内部最晚节点早于 2028-12-17,确保不临期集中变更
6 送企业的最省事做法:一套“可被审核”的证据链,问题一次做干净
我们给客户做这类适配,目标从来不是“把符号画好”,而是把审核问到的证据链提前摆好。
0-2周:把“知道”变成文件
更新适用标准清单:纳入 ISO 15223-1:2021(含 AMD1:2025)
写 1 页影响评估:哪些产品/哪些标签物料受影响、是否触发设计变更
2-6周:把“影响”变成计划
做符号差距清单(SKU-物料-国家-切换节点)
定过渡策略:新品/变更优先按新版;存量按批次切换
设内部最晚切换节点,不要卡着 2028-12-17
6-12周:把“计划”变成证据链
文件控制:版本更改记录、审批、发布、培训
风险管理:RMF 中体现标签变更评估结论与依据
供应链:包材消耗/双版本共存管理,防止混装


